Remoção de nitrogênio
Remoção físico- química de nitrogênio
A remoção de amônia por arraste de ar, também conhecida por stripping, pode ser resumida da seguinte forma:
- ajuste do pH do efluente, para facilitar o arraste de N – NH3;
- agitação com introdução de ar
Em função do pH do efluente , o nitrogênio amoniacal pode ocorrer na água como íon amônio (NH4+) ou gás amônia (NH3-).
NH3 + H2O = NH4+ + OH-
A Figura a seguir apresenta graficamente a distribuição do nitrogênio amoniacal em função do pH.
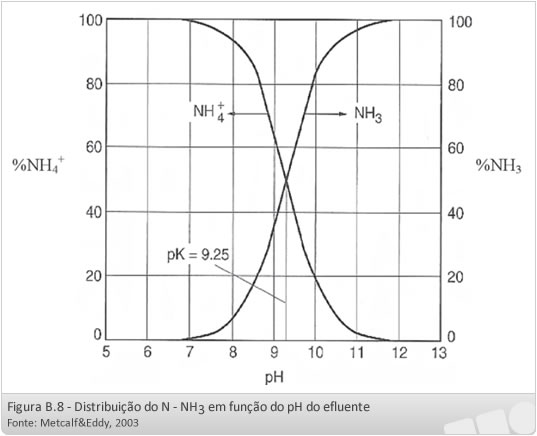
A eficiência de remoção do nitrogênio amoniacal por arraste de ar é extremamente dependente do pH do efluente, o qual determina a parcela que pode ser removida por volatilização para a atmosfera. Isto significa que o nitrogênio amoniacal deve, inicialmente, ser convertido ao gás amônia (pelo ajuste do pH para valores próximo a 11) para posterior transferência para a atmosfera por um determinado fluxo de ar.
A reação também é dependente da temperatura, ou seja, quanto menor for a temperatura, maior será a solubilidade da amônia, portanto, mais difícil de ser removida. Alguns autores justificam a manutenção da temperatura entre 24 e 30°C, entretanto, pode ser também verificado em artigos ou site de fabricantes a indicação de temperaturas maiores, chegando a 60 - 80° C. Valores muito elevados de temperaturas são difíceis de serem mantidos em condições reais de operação, além de representarem custos adicionais.
O ajuste do pH é normalmente realizado com a utilização de cal ou soda cáustica. Como as características dos efluentes são muito variadas, não existe uma solução que se aplique a todos os casos, então, o mais recomendado é realizar testes de bancada antes de definir qual a dosagem mais adequada para o efluente em questão.
A separação do gás amônia é realizada em torres de aeração ou de gotejamento (também denominadas torres de stripping) que são similares a torres de resfriamento.
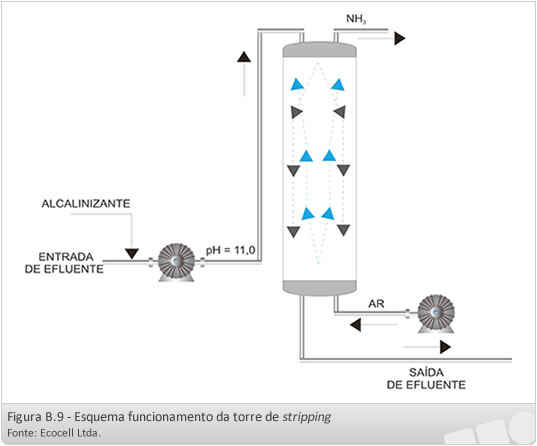

Remoção biológica de Nitrogênio
As formas predominantes são o nitrogênio orgânico e a amônia. Estes dois, conjuntamente, são determinados em laboratório pelo método Kjedahl, constituindo o assim denominado Nitrogênio Kjedahl Total (NKT).
As demais formas de nitrogênio, como nitrito e nitrato, são usualmente de menor importância nos efluentes e de difícil detecção analítica.
Em resumo, tem-se:
NTK = nitrogênio amoniacal + nitrogênio orgânico
NT (nitrogênio total)= N-NH3+ N – org. + NO2 + NO3
Os métodos clássicos de remoção de nitrogênio envolvem dois processos:
- Nitrificação: conversão do nitrogênio amoniacal a nitrato;
- Denitrificação: conversão do nitrato a nitrogênio gasoso.
A nitrificação é um processo biológico que ocorre naturalmente em sistemas onde existam condições aeróbias e a presença de nitrogênio amoniacal. A nitrificação pode ser realizada por microorganismos em leito fixo ou em cultivo suspenso.
O nitrogênio na forma de amônia converte-se em nitrato em duas fases, mediante as bactérias nitrificantes autotróficas, segundo as reações:
1a Reação: NH4+ + 3/2 O2 → NO2- + 2H+ + H2O (Nitrossomonas)
2a Reação: NO2‑ + ½ O2 → NO3- (Nitrobacter)
Reação Total: NH4+ + 2 O2 → NO3- + 2H+ + H2O
Parâmetros importantes na cinética da nitrificação:
- temperatura: 10- 35° ( abaixo de 8° não ocorre)
- pH: entre 7,5 a 8,5 ( ótimo: 8,4)
- Oxigênio dissolvido: > 1,0 mg/L
- Alcalinidade requerida: 7,1 mgCaCO3/mg N amoniacal rem.
- Oxigênio requerido: 4,6 mgO2/mg N amoniacal rem.
- Produção de biomassa: 0,1 g SSV/g N amoniacal rem.
A denitrificação biológica envolve a redução do nitrato a nitrito e do nitrito a nitrogênio gasoso. O nitrito e o nitrato fornecem oxigênio para respiração microbiana da própria reação de denitrificação. Assim sendo, a condição adequada para a denitrificação - oxigênio ausente, mas com nitrato presente, chamada de anóxica.
As reações de obtenção de energia podem representar-se por:
1a reação: 6NO3- + 2CH3OH → 6NO2- + 2CO2 + 4H2O
2a reação: 6NO2- + 3CH3OH → 3N2 + 3CO2 + 3H2O + 6OH-
Reação Total: 6NO3- + 5CH3OH ® 5CO2 + 3N2 + 7H2O + 6OH-
Sistemas biológicos de remoção de Nitrogênio
Os principais sistemas para a remoção biológica de nitrogênio (nitrificação/denitrificação) podem ser resumidos da seguinte forma:
- Pré-denitrificação (remoção de nitrogênio com carbono do esgoto bruto).
- Pós-denitrificação (remoção de nitrogênio com carbono da respiração endógena).
- Processo Bardenpho de quatro estágios.
- Reatores de operação intermitente (batelada).
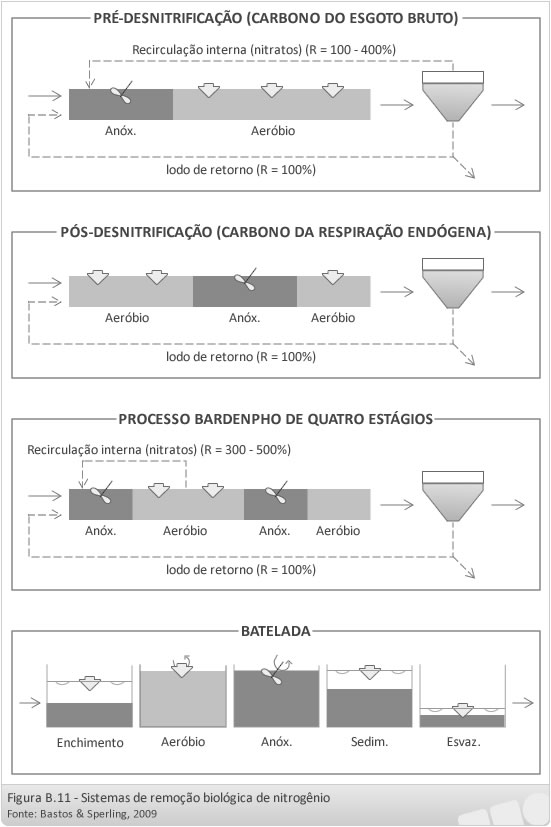
- Pré-denitrificação (remoção de nitrogênio com carbono do esgoto afluente):
- menor tempo de detenção na zona anóxica, comparado ao arranjo de pós-denitrificação;
- redução do consumo de oxigênio, face à estabilização da matéria orgânica utilizando o nitrato como receptor de elétrons na zona anóxica;
- possibilidade da redução do volume da zona aeróbia, em decorrência da estabilização de parte da DBO na zona anóxica;
- não há necessidade de um tanque de reaeração separado, como no arranjo de pós denitrificação.
- Pós nitrificação (Remoção de nitrogênio com carbono da respiração endógena):
- Processo Bardenpho de quatro estágios
- Reatores de operação intermitente (batelada)
O reator possui uma zona anóxica seguida pela zona aeróbia. A nitrificação ocorre na zona aeróbia, conduzindo à formação de nitratos. Os nitratos são direcionados à zona anóxica, por meio de recirculação interna. Na zona anóxica, os nitratos são convertidos a nitrogênio gasoso, escapando para a atmosfera.
As vantagens desse sistema são:
A principal desvantagem é a necessidade da vazão de recirculação interna bastante elevada, o que pode ser economicamente inviável.
O reator compreende uma zona aeróbia seguida por uma zona anóxica e, opcionalmente, uma zona aeróbia final. A remoção de carbono e a produção de nitratos ocorrem na zona aeróbia. Os nitratos formados entram na zona anóxica, onde são reduzidos a nitrogênio gasoso. Dessa forma, não há necessidade de recirculações internas, como no sistema de pré-denitrificação.
A desvantagem é que a denitrificação ocorre em condições endógenas, já que a maior parte do carbono orgânico a ser utilizado pelas bactérias denitrificantes já foi removida na zona aeróbia. Consequentemente, a taxa de denitrificação é menor, o que implica a necessidade de maiores tempos de detenção na zona anóxica, comparado com a alternativa de pré-desnitrificação.
O processo Bardenpho corresponde a uma combinação dos dois arranjos anteriores, compreendendo uma pré-denitrificação e uma pós-denitrificação, além da zona de reaeração final. A eficiência de remoção de nitrogênio é bastante elevada, já que os nitratos não removidos na primeira zona anóxica têm uma segunda oportunidade de serem removidos, na segunda zona anóxica.
A desvantagem é a necessidade de reatores com um volume total maior.
Os sistemas por batelada são operados com etapas cíclicas. Cada ciclo é composto por uma sequência de etapas de enchimento, reação, sedimentação, esvaziamento e, eventualmente, repouso.
Durante o período de enchimento, pode ocorrer alguma remoção de formas oxidadas de nitrogênio (principalmente nitratos), remanescentes do ciclo anterior. Tem-se, portanto, uma pré-desnitrificação com carbono orgânico do esgoto afluente.
Após a etapa de reação aeróbia, tem-se uma etapa anóxica, na qual ocorre a pós-desnitrificação, em condições endógenas.
A vantagem do sistema é a sua simplicidade conceitual, dispensando decantadores e recirculações separadas.
A desvantagem é que o equipamento de aeração só funciona parte do tempo. Portanto, nos períodos de aeração a transferência de oxigênio terá que ser maior. Por essa razão, a quantidade de aeradores num sistema de bateladas necessita ser maior (maior potência instalada) que num sistema de fluxo contínuo sob as mesmas condições operacionais.

Dimensionamento básico
Os sistemas biológicos descritos na aula passada estão basicamente dependentes das condições ambientais anteriormente citadas. Porém, talvez a mais importante seja o fornecimento da quantidade de oxigênio necessária a nitrificação: 4,6 mgO2/mg N amoniacal rem.
No dimensionamento básico é necessário calcular a necessidade de fornecimento de oxigênio (RO: requisito de oxigênio) para depois calcular o tamanho do aerador (ou outro sistema de fornecimento de oxigênio), denominado nesse estudo como RE (requisito energético).
Exemplos:
Quantos kg de oxigênio são necessários para nitrificar 100 kg de N – amoniacal?
100 kg NH3x 4,6 kg O2/Kg NH3 = 460 kg de O2
Considerando um efluente industrial com vazão de 100 m³.d-1 e com N amoniacal de 100 mg.L-1, qual o RO para atender ao padrão de emissão de 20 mg,L-1?
- Q x (Ne – Ns) x 4,6 = 100 m3.d-1 x (100 mg.L-1 - 20 mg.L‑1) x 4,6 = 38.600 g.d-1 ou 38,6 kg O2.d-1
E o RE para esse caso, qual seria?
- Primeiro selecione a aerador com base nas informações do fabricante: 1,8 kg O2/kW/h
- Depois aplique o coeficiente de segurança, para operação em escala real: 50%
- Então, na verdade o aerador fornece 0,9 kgO2/kW/h (1,8 kgO2/kW/h x 50%) ou 21,6 kgO2/kW/d
Sendo assim, podemos calcular da seguinte forma:
21,6 kg O2/d - 1 kW
38,6 kg O2/d - X
Está claro?
Então, por fim, imagine a seguinte situação: Uma empresa já possui um sistema de tratamento aeróbio, dimensionado para a remoção de matéria-orgânica. A intenção do projetista é remover N de forma eficiente nesse mesmo reator, portanto, é necessário, pelo menos, aumentar o fornecimento de Oxigênio através do uso de aeradores. Sendo assim, determine o RO e o RE com base nas informações abaixo:
Q = 10 m³.h-1, DBOe = 1.000 g.m-3, DBOs = 200 g.m-3, NTKe 120 g.m-3 . NTKs = 20 g.m-3
- determine a carga de MO a ser removida: Q x (DBOe – DBOs) = 192 kg O2.d-1
- determine a carga de N a ser removida: Q x (Ne – Ns) x 4,6 = 110,4 kg O2.d-1
- o RO é a soma de 192 kg O2.d-1 e 110,4 kg O2.d-1 = 302,4 kg O2.d-1
- selecione a aerador com base nas informações do fabricante: 1,2 kg O2/kW/h
- depois aplique o coeficiente de segurança, para operação em escala real: 50%
- então, na verdade o aerador fornece 0,6 kgO2/kW/h (1,2 kgO2/kW/h x 50%) ou 14,4 kgO2/kW/d
- agora, é só calcular o RE:
14,4 kg O2/d - 1 kW
302,4 kg O2/d - X
Resposta: 21 kW ou aprox. 28 cv